Jean-Christophe Quillet, Michael Siani-Rose, Robert McKee, Bonni Goldstein, Myiesha Taylor, Itzhak Kurek*
Sci Rep. 2023;13:13022.
Published online 2023 Aug 22. doi: 10.1038/s41598-023-40073-0
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10444802/
Πληροφορίες συγγραφέων
Cannformatics, Inc., 3859 Cesar Chavez St, San Francisco, CA 94131, ΗΠΑ *email: itzhak@cannformatics.com
Σημειώσεις άρθρου
Λήψη 2023 16 Απριλίου, Αποδεκτό 3 Αυγούστου 2023
Σχετικά δεδομένα
Δήλωση διαθεσιμότητας δεδομένων
Τα σύνολα δεδομένων που χρησιμοποιούνται ή/και αναλύονται σε αυτήν τη μελέτη είναι διαθέσιμα από τον αντίστοιχο συγγραφέα κατόπιν εύλογου αιτήματος.
Περίληψη
“Η διαταραχή του φάσματος του αυτισμού (ΔΑΦ /Autism spectrum disorder, ASD) είναι μια νευροαναπτυξιακή κατάσταση που επηρεάζει τη συμπεριφορά, την επικοινωνία, την κοινωνική αλληλεπίδραση και τις μαθησιακές ικανότητες. Η θεραπεία με ιατρική χρήση της κάνναβης (Medical Cannabis, MC) μπορεί να μειώσει τα κλινικά συμπτώματα σε άτομα με ΔΑΦ. Οι βιοδείκτες που ανταποκρίνονται στην κάνναβη είναι μεταβολίτες που βρίσκονται στο σάλιο και αλλάζουν ως απόκριση στη θεραπεία με MC. Προηγουμένως δείξαμε τα επίπεδα αυτών των βιοδεικτών σε παιδιά με ΔΑΦ που αντιμετωπίστηκαν επιτυχώς με MC να μετατοπίζονται προς τα φυσιολογικά επίπεδα που ανιχνεύθηκαν σε τυπικά αναπτυσσόμενα παιδιά και δυνητικά μπορεί να ποσοτικοποιηθεί ο αντίκτυπος. Εδώ, δοκιμάσαμε για πρώτη φορά τις δυνατότητες των τεχνικών μηχανικής μάθησης που εφαρμόζονται στο δυναμικό, υψηλής ανάλυσης και πλούσιο σύνολο στοιχείων βιοδεικτών που ανταποκρίνονται στην κάνναβη από περιορισμένο αριθμό παιδιών με ΔΑΦ πριν και μετά τη θεραπεία με MC και μια ομάδα TD για τον εντοπισμό : (1) βιοδείκτες που διακρίνουν τις ομάδες ΔΑΦ και TD. (2) μη κανναβινοειδή φυτικά μόρια με συνεργατικά αποτελέσματα, και (3) βιοδείκτες που σχετίζονται με συγκεκριμένα κανναβινοειδή. Βρήκαμε: (1) η λυσοφωσφατιδυλαιθανολαμίνη μπορεί να διακρίνει μεταξύ των ομάδων ΔΑΦ και TD. (2) νέα φυτοχημικά συμβάλλουν στα θεραπευτικά αποτελέσματα της θεραπείας με MC με την αναστολή της ακετυλοχολινεστεράσης, και (3) Οι βιοδείκτες που ανταποκρίνονται στην κάνναβη που σχετίζονται με THC και CBD είναι δύο ξεχωριστές ομάδες, ενώ η CBG σχετίζεται με ορισμένους βιοδείκτες και από τις δύο ομάδες”.
Θεματικοί όροι: Metabolomics, Machine learning, Biomarkers (Μεταβολομική, Μηχανική μάθηση, Βιοδείκτες, αντίχτοιχα)
Εισαγωγή
Η διαταραχή του φάσματος του αυτισμού (ΔΑΦ / Autism spectrum disorder, ASD) είναι ένα σύνολο ετερογενών νευροαναπτυξιακών καταστάσεων που επηρεάζουν την κοινωνική αλληλεπίδραση και την επικοινωνία με καθορισμένα στερεότυπα πρότυπα συμπεριφοράς[1]. Είναι μια δια βίου πάθηση με έναρξη ήδη από το πρώτο ή το δεύτερο τρίμηνο που συχνά συνυπάρχει με νοητικές αναπηρίες, ψυχιατρικές παθήσεις, νευρο-φλεγμονές ή/και γαστρεντερικές διαταραχές[2-5].
Η διάγνωση και η αξιολόγηση της αποτελεσματικότητας της θεραπείας αποτελούν πρόκληση λόγω της κλινικής φαινοτυπικής ετερογένειας της ΔΑΦ και επί του παρόντος βασίζονται αποκλειστικά στην υποκειμενική αξιολόγηση από αναπτυξιακούς παιδιάτρους, νευρολόγους ή ψυχολόγους. Ως εκ τούτου, οι βαθμολογίες του εργαλείου έρευνας παρατήρησης δεν είναι συγκρίσιμες μεταξύ των ασθενών και δεν παρέχουν πληροφορίες σχετικά με την υποκείμενη παθοφυσιολογία της ΔΑΦ. Δεδομένου ότι η εμφάνιση της ΔΑΦ πυροδοτείται τόσο από γενετικούς όσο και από περιβαλλοντικούς παράγοντες μέσω ενός καταρράκτη βιοχημικών γεγονότων που οδηγεί σε πλειοτροπικές μεταβολικές ανωμαλίες με υψηλή μεταβλητότητα μεταξύ των ατόμων, είναι δύσκολο να εντοπιστούν βιοδείκτες ΔΑΦ[6]. Το γεγονός ότι ο κίνδυνος απόκτησης δεύτερου παιδιού με ΔΑΦ είναι 25 φορές υψηλότερος για οικογένειες που έχουν ήδη παιδί με ΔΑΦ σε σύγκριση με οικογένειες με τυπικά αναπτυσσόμενο παιδί (typically-developing, TD) υποδηλώνει έντονα τη συμμετοχή γενετικών παραγόντων[7]. Ωστόσο, οι γενετικοί βιοδείκτες που σχετίζονται ειδικά με τη ΔΑΦ δεν έχουν ταυτοποιηθεί ούτε χρησιμοποιούνται συστηματικά για διαλογή. Μη φυσιολογικά επίπεδα πρωτεϊνών και μεταβολιτών που σχετίζονται με το οξειδωτικό στρες, τη φλεγμονή, τη μιτοχονδριακή δυσλειτουργία και τη δυσλειτουργία του ανοσοποιητικού έχουν εντοπιστεί και χαρακτηριστεί στη ΔΑΦ τις τελευταίες δύο δεκαετίες[8]. Ωστόσο, η υψηλή μεταβολική μεταβλητότητα μεταξύ ατόμων με ΔΑΦ και συννοσηρότητα που σχετίζεται με άλλες διαταραχές έχουν περιορίσει την ανάπτυξη αξιόπιστων πρωτεομικών και μεταβολικών βιοδεικτών για τη διάγνωση και την αξιολόγηση της θεραπείας.
Η μηχανική μάθηση (machine learning, ML) είναι ένα υποπεδίο της τεχνητής νοημοσύνης (artificial intelligence, AI) στο οποίο μια ποικιλία στατιστικών και υπολογιστικών μεθόδων εφαρμόζεται σε μεγάλα και πολύπλοκα σύνολα δεδομένων προκειμένου να αναπτυχθούν ή/και να προσαρμοστούν προγνωστικά μοντέλα από μίμηση ανθρώπινων διαδικασιών αναγνώρισης προτύπων[9]. Η ML απαιτεί ένα σύνολο δεδομένων εκπαίδευσης που αποτελείται από σημεία δεδομένων, καθένα από αυτά θεωρείται ως μια ενιαία παρατήρηση από ένα πείραμα που περιγράφεται από τον αριθμό των χαρακτηριστικών. Ένας επαρκής αριθμός εκπαιδευμένων χαρακτηριστικών επιτρέπει την ανάπτυξη ενός μοντέλου που προβλέπει το αποτέλεσμα. Οι τεχνικές ML έχουν εφαρμοστεί με επιτυχία σε μελέτες μεταβολομικής για τον εντοπισμό των εξής: τη μεταβολική υπογραφή σοβαρών περιπτώσεων COVID-19, την ταξινόμηση της μικροχλωρίδας του ανθρώπινου εντέρου, μεταβολικές αλλαγές στην ανθρώπινη εγκυμοσύνη, μόλυνση από γρίπη, νεφρικό καρκίνωμα (ακρίβεια 88%), διαβητική νεφρική νόσο, παραγαγγλιώματα κεφαλής και τραχήλου (ακρίβεια 99,2%), καρκίνος της ουροδόχου κύστης σε πρώιμο στάδιο (έως 95% ακρίβεια) και τα μεταβολομικά σημάδια των υποτύπων μείζονος καταθλιπτικής διαταραχής[10]. Οι Chen et al.[11] συνδύασαν μη στοχευμένη μεταβολομική ούρων με βάση το GC/MS σε δείγματα που συλλέχθηκαν από μια ομάδα παιδιών με ΔΑΦ και μια ομάδα ελέγχου TD με τον αλγόριθμο XGBoost για τον εντοπισμό 20 πιθανών μεταβολικών βιοδεικτών για τη διάκριση μεταξύ των ομάδων, οι οποίες χαρτογραφήθηκαν σε ποικιλία μεταβολικών οδών.
Η θεραπεία με ιατρική χρήση της κάνναβης (MC) αναδεικνύεται ως μια πολλά υποσχόμενη λύση για τη θεραπεία παιδιών με ΔΑΦ, ειδικά ελλείψει εγκεκριμένων φαρμάκων που αποτυγχάνουν να αντιμετωπίσουν τα βασικά συμπτώματα της ΔΑΦ. Βελτιώσεις στις δεξιότητες κοινωνικής επικοινωνίας παιδιών και εφήβων με ΔΑΦ που υποβλήθηκαν σε θεραπεία με κάνναβη πλούσια σε CBD αναφέρθηκαν πρόσφατα από τους Hacohen et al.[12], ενώ αναφέρθηκαν βελτιώσεις στις συμπεριφορικές εκρήξεις, το άγχος και την επικοινωνία για παιδιά με ΔΑΦ που έλαβαν σκευάσματα χαμηλής περιεκτικότητας σε τετραϋδροκανναβινόλη (THC ) και σκευάσματα υψηλής περιεκτικότητας σε κανναβιδιόλη (CBD)[13]. Αυτές οι μελέτες χρησιμοποίησαν υποκειμενικές αξιολογήσεις, περιορίζοντας την ικανότητα ποσοτικοποίησης του αντίκτυπου της θεραπείας με MC. Με την αύξηση της θεραπείας με MC σε παιδιά και εφήβους με ΔΑΦ, υπάρχει μια αυξανόμενη ανάγκη για αντικειμενικά, ποσοτικά δεδομένα για τον προσδιορισμό της αποτελεσματικότητας, της ασφάλειας, του μηχανισμού δράσης και των κυτταρικών στόχων των κανναβινοειδών.
Πρόσφατα αναφέραμε μια νέα φαρμακομεταβολομική προσέγγιση στην οποία τα επίπεδα των μεταβολιτών, ειδικά των βιοδεικτών που ανταποκρίνονται στην κάνναβη, σε παιδιά με ΔΑΦ που υποβάλλονται σε θεραπεία με MC μετατοπίζονται προς τα φυσιολογικά επίπεδα που ανιχνεύονται σε τυπικά αναπτυσσόμενα (TD) παιδιά χωρίς θεραπεία[14,15]. Σε αυτές τις έρευνες, εντοπίσαμε μια πιθανή σχέση μεταξύ των βιοδεικτών που ανταποκρίνονται στην κάνναβη και της μιτοχονδριακής δυσλειτουργίας, των αλλαγών στους νευροδιαβιβαστές, της ανώμαλης νευρωνικής ανάπτυξης, της νευροφλεγμονής, της βιοενέργειας και του οξειδωτικού στρες. Είναι σημαντικό ότι οι βιοδείκτες που ανταποκρίνονται στην κάνναβη ποσοτικοποίησαν τον αντίκτυπο της θεραπείας με MC στα παιδιά με ΔΑΦ, ρίχνοντας φως στην υποκείμενη παθοφυσιολογία της ΔΑΦ και υποδεικνύοντας έναν πιθανό μηχανισμό δράσης (mechanism of action, MOA) των κανναβινοειδών.
Σε προηγούμενες μελέτες μας[14,15] χρησιμοποιήσαμε σκληρά κωδικοποιημένους αλγόριθμους για να αναγνωρίσουμε και να ταξινομήσουμε βιοδείκτες που μετατοπίζονται αποκλειστικά προς τα φυσιολογικά επίπεδα. Εδώ διερευνούμε τις δυνατότητες της βάσης δεδομένων βιοδεικτών που ανταποκρίνεται στην κάνναβη, η οποία περιέχει μεγάλο αριθμό μεταβολιτών που ανιχνεύονται σε περιορισμένο αριθμό παιδιών με ΔΑΦ, ανεξάρτητα από τα φυσιολογικά αποτελέσματα, και ελέγχους TD, για εφαρμογές ML που δίνουν κυρίως νέους υποψήφιους βιοδείκτες που παραβλέπονται σε προηγούμενες μελέτες. Εκπαιδεύσαμε μοντέλα ενίσχυσης κλίσης για: (1) διάκριση ατόμων με ΔΑΦ από την ομάδα ελέγχου πριν και μετά τη θεραπεία με MC. (2) ταυτοποίηση μη κανναβινοειδών φυτικών μορίων (φυτοχημικά) με φαρμακευτικά οφέλη που συμβάλλουν στη συνεργατική επίδραση που είναι γνωστή ως η “συνδυαστική επίδραση” (entourage effect)[16]. (3) διάκριση συγκεκριμένων βιοδεικτών που ανταποκρίνονται σε THC, CBD και κανναβιγερόλη (CBG) και (4) παροχή πληροφοριών σχετικά με τον ειδικό αντίκτυπο των κανναβινοειδών σε μη ισορροπημένες μεταβολικές οδούς σε παιδιά με ΔΑΦ. Τα μοντέλα ML που βασίζονται σε Gradient Boosting αποδίδουν καλά με δεδομένα υψηλών διαστάσεων όπου ο αριθμός των χαρακτηριστικών υπερβαίνει τον αριθμό των δειγμάτων και μας παρέχουν μια απλή μέθοδο για να ταξινομήσουμε αυτά τα χαρακτηριστικά, τους μεταβολίτες, σύμφωνα με τη σχετική συνεισφορά τους στην πρόβλεψη για κάθε εργασία.
Τα προκαταρκτικά αποτελέσματα που παρουσιάζονται σε αυτή τη μελέτη καταδεικνύουν τη δυνατότητα της βάσης δεδομένων βιοδεικτών που ανταποκρίνονται στην κάνναβη σε συνδυασμό με εφαρμογές ML να παρέχει πληροφορίες για τη φαρμακοκινητική, τη φαρμακοδυναμική και την MOA των κανναβινοειδών και τους στόχους σε διαταραχές που σχετίζονται με το ενδοκανναβινοειδές σύστημα (ΕΚΣ / endocannabinoid system, ECS) και τον εντοπισμό νέα φυτοσυστατικά κάνναβης με πιθανούς θεραπευτικούς ρόλους.
Αποτελέσματα
Πιθανά χαρακτηριστικά βάσης δεδομένων βιοδεικτών που ανταποκρίνονται στην κάνναβη
Δεκαπέντε παιδιά (μέση ηλικία 9,4 έτη) συμμετείχαν στην ομάδα ΔΑΦ και 10 παιδιά με παρόμοια ηλικιακή κατανομή (μέση ηλικία 9,3 έτη) συμμετείχαν στην ομάδα ελέγχου χωρίς θεραπεία με TD, όπως περιγράφηκε προηγουμένως λεπτομερώς[14,15]. Στην ομάδα ΔΑΦ 11 παιδιά εμφάνισαν σοβαρό εύρος, 2 παιδιά εμφάνισαν μέτριο εύρος και 2 παιδιά εμφάνισαν ένα ήπιο εύρος κοινωνικής αναπηρίας που σχετίζεται με ΔΑΦ όπως αναφέρεται από τις αξιολογήσεις γονέων (SRS-2), όπως περιγράφεται λεπτομερώς από τους Siani-Rose et al.[14] (Suppl 2).
Εφαρμόσαμε εφαρμογές ML σε δεδομένα πηγής για κάθε παιδί που περιέχουν τις απόλυτες τιμές 645 μεταβολιτών που ανιχνεύθηκαν στο σάλιο που συλλέχθηκε από τους συμμετέχοντες στη μελέτη με dual scan capillary electrophoresis time-of-flight-mass spectrometry (CE-TOF-MS) και rapid resolution liquid chromatography-time-of-flight-mass spectrometry
(RRLC-TOF-MS)[14,15]. Τα δείγματα χαρακτηρίστηκαν σε παιδιά με ΔΑΦ πριν από τη θεραπεία με MC ως PRE και περίπου 90 λεπτά μετά τη θεραπεία με MC ως PEAK και ένα μεμονωμένο δείγμα από παιδιά στην ομάδα ελέγχου TD που δεν υποβλήθηκε σε θεραπεία ως (TD). Για ορισμένα παιδιά με ΔΑΦ, συλλέξαμε επίσης δείγματα που ονομάστηκαν Post-1 και Post-2 περίπου 180 και 270 λεπτά μετά τη θεραπεία με MC, αντίστοιχα. Αυτά τα δεδομένα συμπληρώθηκαν με τα αριθμητικά δεδομένα που φαίνονται στον Πίνακα 1, στον οποίο οι δόσεις από τα κύρια κανναβινοειδή που χρησιμοποιήθηκαν στη θεραπεία MC ομαδοποιήθηκαν σε κλίμακες που κυμαίνονται από 0–3 (THC), 0–4 (CBD) και 0–2 (CBG). και οι έρευνες αξιολόγησης συμπεριφοράς γονέων στο PRE και το PEAK ομαδοποιήθηκαν σε κλίμακα 0-3. Η THC ήταν μέρος της θεραπείας για το 80% των παιδιών, η CBD ήταν μέρος της θεραπείας για το 67% των παιδιών και η CBG ήταν μέρος της θεραπείας για το 33% των παιδιών. Όλα τα παιδιά έπαιρναν THC ή CBD, με το 47% να λαμβάνει και THC και CBD και το 7% να λαμβάνει THC, CBD και CBG. Αυτή η κατάταξη περιελάμβανε όλους τους πρακτικούς συνδυασμούς THC, CBD και CBG με επαρκή στατιστική ισχύ. Σύμφωνα με έρευνες αξιολόγησης συμπεριφοράς, οι γονείς της ομάδας ΔΑΦ ανέφεραν πλήρη και μερική βελτίωση μετά τη θεραπεία με MC (PEAK vs PRE) στο 80% των παιδιών.
Οι διαφορικά εκφρασμένοι δυνητικοί βιοδείκτες που ανταποκρίνονται στην κάνναβη διακρίνουν κατηγορίες παιδιών με ΔΑΦ
Χρησιμοποιώντας την ML Gradient Boosting για ταξινόμηση πολλαπλών κατηγοριών των δειγμάτων μεταβολομικής και την προκύπτουσα κατάταξη σπουδαιότητας των χαρακτηριστικών για την πρόβλεψη μοντέλων, δημιουργήσαμε 3 κατηγορίες πιθανών βιοδεικτών που περιγράφονται παρακάτω και στην Εικ. 1Α.
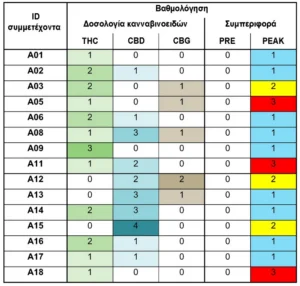
Πίνακας 1. Αριθμητικές κλίμακες των κύριων κανναβινοειδών και έρευνες αξιολόγησης συμπεριφοράς που χρησιμοποιούνται για σύνολα δεδομένων παιδιών με ΔΑΦ. Οι δόσεις κανναβινοειδών ομαδοποιήθηκαν σύμφωνα με τις ακόλουθες συγκεντρώσεις:
THC: (0) Όχι, (1) 0,05–5,00mg, (2) 5,05–15,00mg και (3) > 15,05mg
CBD: (0) Όχι, (1) 1–0mg, (2) 31-84mg, (3) 85–100mg και (4) > 100mg
CBG: (0) Όχι, (1) 1–49mg, (2) > 50mg
Η ένταση χρώματος αντιπροσωπεύει την κατάταξη της ομάδας, χωρίς χρώμα στο 0. Η κατάταξη συμπεριφοράς στα χρονικά σημεία PRE και PEAK αριθμήθηκε και κωδικοποιήθηκε το χρώμα ως εξής: (1, μπλε) βελτιώθηκε. (2, κίτρινο) μερικώς βελτιωμένο και (3, κόκκινο) επιδεινώθηκε.
(1) ASD PRE/ASD PEAK
Εννέα δυνητικοί βιοδείκτες που ανταποκρίνονται στην κάνναβη ταυτοποιήθηκαν ως υποψήφιοι για διάκριση πριν από τη θεραπεία με MC (PRE) ή μετά τη θεραπεία με MC (PEAK), συμπεριλαμβανομένων των νευροδραστικών ενώσεων ανανδαμίδιο (anandamide, AEA), λυσοφωσφατιδυλαιθανολαμίνη (lysophosphatidylethanolamine, LysoPE18:1), τα συνδεδεμένα με νευροεκφυλιστικά λιπίδια λυσοφωσφατιδυλοχολίνης (lipids lysophosphatidylcholine, LysoPC18:0 και LysoPC16:0) και σφιγγοσίνη (sphingosine) και οι ενώσεις λιπιδίων/λιπιδικής οδού υδροξυγλουταρικό οξύ (hydroxy glutaric acid), ακετυλ-σφιγγοσίνη (acetyl sphingosine), διαιθανολαμίνη (diethanolamine, dETA) και φωσφορική αιθανολαμίνη (ethanolamine phosphate, ETA-P).
(2) ASD PRE και ASD PEAK
Δέκα πιθανοί βιοδείκτες που ανταποκρίνονται στην κάνναβη προσδιορίστηκαν ως υποψήφιοι για τη διάκριση όλων των παιδιών με θεραπεία ΔΑΦ, όπου τόσο το PRE όσο και το PEAK συνδυάζονται σε μια ενιαία σειρά, συμπεριλαμβανομένων των νευροδραστικών ενώσεων AEA, LysoPE(18:1), ομοβανιλικό οξύ (homovanilic acid, HVA), κορτιζόλη (cortisol), λιπίδια παλμιτοϋλ-καρνιτίνης (lipids palmitoyl-carnitine), αριχιδικό οξύ (arichidic acid), 2-υδροξυ βουτυρικό οξύ (2-hydroxy butyric acid, 2-HBA), λακτοζυλοκεραμίδιο (lactosyl ceramide) και το στεροειδές/παράγωγο λανοστερόλη (lanosterol) και η 3-θειική δεϋδροϊσοανδροστερόνη (Dehydroisoan-drosterone 3-sulfate, DHEA-S).
(3) TD/ASD PRE/ASD PEAK
Επτά δυνητικοί βιοδείκτες που ανταποκρίνονται στην κάνναβη ταυτοποιήθηκαν ως υποψήφιοι για τη διάκριση της ομάδας ελέγχου TD και των παιδιών με ΔΑΦ στο PRE και PEAK, συμπεριλαμβανομένων των νευροενεργών LysoPE(18:1), της σφιγγοσίνης, των λιπιδίων που σχετίζονται με νευροεκφυλιστικά LysoPC18:0 και LysoPC16:0, σφιγγομυελίνη (sphingomyelin), σφιγγανίνη (sphinganine) και εικοσατριενοϊκό οξύ (eicosa-trienoic acid, DGLA).
Το LysoPE(18:1) ήταν ο μόνος δυνητικός βιοδείκτης που ανταποκρίνεται στην κάνναβη για τη διάκριση και των 3 κατηγοριών, όπως υποδεικνύεται από το διάγραμμα Venn (Εικ. 1Α). Τα συνολικά υψηλά επίπεδα LysoPE(18:1) και η υψηλή μεταβλητότητα δείγματος (Εικ. 1Β) που βρέθηκαν σε παιδιά με ΔΑΦ σε PRE (μπλε) μειώθηκαν στο PEAK (ανοιχτό μπλε), αλλά δεν έφτασαν τα χαμηλά επίπεδα και τη χαμηλή μεταβλητότητα που εντοπίστηκαν στο TD ομάδα (πράσινο). Αυτό το μοτίβο έκφρασης ταιριάζει στα κριτήρια ενός βιοδείκτη που μπορεί να χρησιμοποιηθεί για τη διάκριση και των τριών κατηγοριών, δηλαδή ASD PRE/ASD PEAK, ASD PRE και ASD PEAK και TD/ASD PRE/ASD PEAK.
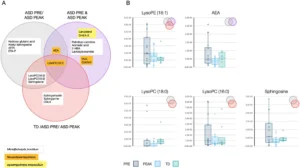
Εικόνα 1. Προσδιορισμός πιθανών βιοδεικτών που ανταποκρίνονται στην κάνναβη της ΔΑΦ που διακρίνουν κατηγορίες ασθενών. (Α) Διάγραμμα Venn που απεικονίζει τους μοναδικούς και επικαλυπτόμενους διαφορικά εκφραζόμενους βιοδείκτες που ανταποκρίνονται στην κάνναβη που βρέθηκαν στις κατηγορίες ασθενών με ASD PRE/ASD PEAK, ASD PRE και ASD PEAK και TD/ ASD PRE/ASD PEAK. Οι ρόλοι των βιοδεικτών (μεταβολισμός λιπιδίων, νευροδραστηριότητα και δραστηριότητα στεροειδών) είναι κωδικοποιημένοι με χρώμα (λευκό, πορτοκαλί και κίτρινο, αντίστοιχα). (Β) Επίπεδα πιθανών βιοδεικτών που ανταποκρίνονται στην κάνναβη που βρέθηκαν σε παιδιά με ΔΑΦ σε PRE (μπλε) και PEAK (ανοιχτό μπλε) και ομάδα TD (πράσινο) στις επικαλυπτόμενες κατηγορίες που περιγράφονται στο (Α). Κάθε περιοχή πλαισίου περικλείεται οριζόντια από το κάτω και το άνω τεταρτημόριο και υποδεικνύεται η διάμεσος (συμπαγή οριζόντια γραμμή εντός του πλαισίου). Οι επικαλυπτόμενες κατηγορίες υποδεικνύονται στην επάνω δεξιά γωνία.
Το ενδοκανναβινοειδές AEA, το οποίο λειτουργεί ως νευροδιαβιβαστής και παράγεται και απελευθερώνεται “κατ’ απαίτηση”[14], βρέθηκε να επικαλύπτει τις κατηγορίες ASD PRE/ASD PEAK και ASD PRE και ASD PEAK, με τα συνολικά χαμηλότερα επίπεδα και τη χαμηλότερη μεταβλητότητα στα παιδιά με ASD στο PEAK.
Οι πιθανοί βιοδείκτες που ανταποκρίνονται στην κάνναβη με βάση τα λιπίδια LysoPC(18:0), LysoPC(16:0) και την σφιγγοσίνη αλληλεπικαλύπτονται ως προς την ικανότητα διάκρισης των κατηγοριών ASD PRE/ASD PEAK και TD /ASD PRE/ASD PEAK μειώνοντας τα υψηλά επίπεδα και υψηλή μεταβλητότητα δείγματος στο PRE σε χαμηλά επίπεδα και χαμηλή μεταβλητότητα δείγματος στο PEAK, φτάνοντας σε ένα εύρος και μεταβλητότητα δείγματος πιο κοντά στα επίπεδα που λαμβάνονται στην ομάδα ελέγχου TD.
Οι φυτικοί μεταβολίτες που εκφράζονται διαφορικά διακρίνουν κατηγορίες ασθενών
Η προσέγγιση που περιγράφεται παραπάνω εντόπισε με επιτυχία φυτικούς μεταβολίτες για τη διάκριση κατηγοριών παιδιών με ΔΑΦ (Εικ. 2Α). Επτά διατροφικά φυτοχημικά, όπως η φλαβόνη (flavone), η ρουτίνη (rutin) (κερκετίνη-3-ρουτινοσίδη / quercetin-3-rutinoside), η βιτεξίνη (vitexin) (απιγενίνη 8-γλυκοσίδη / apigenin 8-glucoside), η ναρινγενίνη (naringenin), η ζεαξανθίνη (zeaxanthin), το κοροσολικό οξύ (corosolic acid) και η σιτοστερόλη (sitosterol) εντοπίστηκαν σε παιδιά με ΔΑΦ στο PEAK (Εικ. 2Β). Η σιτοστερόλη ήταν η πιο άφθονη διατροφική φυτοχημική ουσία που εντοπίστηκε στο σάλιο 10 παιδιών με ΔΑΦ. Η ρουτίνη, η βιτεξίνη και η ναρινγενίνη ήταν λιγότερο άφθονα και ανιχνεύθηκαν το καθένα μόνο σε 5, 4 και 4 παιδιά (αντίστοιχα). Το κοροσολικό οξύ ήταν το μόνο διατροφικό φυτοχημικό που ανιχνεύθηκε τόσο στην ομάδα ελέγχου ΔΑΦ όσο και στην ομάδα ελέγχου TD και εμφάνισε ελαφρώς αυξημένη ποσότητα σε PEAK έναντι PRE προς τα επίπεδα που παρατηρήθηκαν σε άτομα με TD.
Όπως υποδεικνύεται στο διάγραμμα Venn στην Εικ. 2Α, η ρουτίνη επικαλύπτει τις κατηγορίες ASD PRE/ASD PEAK και TD/ASD PRE/ ASD PEAK και η σιτοστερόλη επικαλύπτει τις ASD PRE και ASD PEAK και TD/ASD PRE/ASD PEAK. Η χρονοεξαρτώμενη ανίχνευση βιτεξίνης σε δείγματα σάλιου του παιδιού Α18 και ρουτίνης σε δείγματα σάλιου του παιδιού Α16 (Εικ. 2C, D αντίστοιχα) έδειξε ένα διαφορετικό πρότυπο βιοδιαθεσιμότητας στο οποίο η βιτεξίνη αποικοδομείται ταχύτερα από τη ρουτίνη. Ως εκ τούτου, τα ανιχνευμένα επίπεδα ρουτίνης στο σάλιο παιδιών με ΔΑΦ στο PRE θα μπορούσαν να είναι αποτέλεσμα προηγούμενης θεραπείας.
Ο αντίκτυπος των κύριων κανναβινοειδών στη διαφορική εκφρασμένη δυνητική κάνναβη, ανταποκρινόμενοι βιοδείκτες που διακρίνουν κατηγορίες παιδιών με ΔΑΦ
Χρησιμοποιώντας ML Gradient Boosting για ταξινόμηση πολλαπλών κατηγοριών των δειγμάτων μεταβολομικής και την προκύπτουσα κατάταξη σπουδαιότητας των χαρακτηριστικών, αναλύσαμε τη συγκεκριμένη συμβολή των THC, CBD και CBG που βρέθηκε στη θεραπεία MC που περιγράφεται στον Πίνακα 1 σε ένα σύνολο δεδομένων 645 μεταβολιτών ανιχνεύθηκε σε 30 δείγματα σάλιου από 15 παιδιά με ΔΑΦ σε χρονικά σημεία PRE και PEAK. Όπως φαίνεται στην Εικ. 3, η THC συσχετίστηκε με την απόκριση 11 πιθανών βιοδεικτών που ανταποκρίνονται στην κάνναβη που αντιπροσωπεύουν λιπίδια, νευροενεργά μόρια και στεροειδή (5, 5 και 1 αντίστοιχα), συμπεριλαμβανομένων των ενδοκανναβινοειδών AEA και 2-αραχιδονοϋλογλυκερόλης (2-arachidonoylglycerol, 2-AG). Η CBD συσχετίστηκε με 7 πιθανούς βιοδείκτες που ανταποκρίνονται στην κάνναβη με ρόλους στον μεταβολισμό των λιπιδίων, τη νευροδραστηριότητα και τον μεταβολισμό των πρωτεϊνών (5, 1 και 1 αντίστοιχα). Οι 11 δυνητικοί βιοδείκτες που ανταποκρίνονται στην THC κάνναβης δεν αλληλεπικαλύπτονται με τους 7 δυνητικούς βιοδείκτες που ανταποκρίνονται στην CBD κάνναβης. Η CBG συσχετίστηκε στην απόκριση 15 πιθανών βιοδεικτών που ανταποκρίνονται στην κάνναβη με ρόλους στον μεταβολισμό των λιπιδίων και τη νευροδραστηριότητα (11 και 4 αντίστοιχα). Τρεις δυνητικοί βιοδείκτες που ανταποκρίνονται στην CBG κάνναβης επικαλύπτονται με την THC, συμπεριλαμβανομένου του ενδοκανναβινοειδούς 2-AG, της δι-αιθανολαμίνης (dETA) και της τρι-αιθανολαμίνης (tri-ethanolamine, tETA) και ένας δυνητικός βιοδείκτης CBG που ανταποκρίνεται στην κάνναβη, η 3-φωσφορική γλυκερόλη (glycerol 3-phosphate, G3P), που επικαλύπτεται με την CBD.
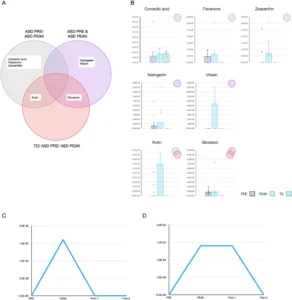
Εικόνα 2. Προσδιορισμός φυτικών μη κανναβινοειδών δευτερογενών μεταβολιτών (διαιτητικά φυτοχημικά) που διακρίνουν κατηγορίες ασθενών. (Α) Διάγραμμα Venn που απεικονίζει τα μοναδικά και επικαλυπτόμενα διατροφικά φυτοχημικά που βρίσκονται στις κατηγορίες ασθενών ASD PRE/ASD PEAK, ASD PRE και ASD PEAK και TD/ ASD PRE/ASD PEAK. Οι διατροφικές φυτοχημικές λειτουργίες (λιπίδια, νευροδραστικές και στεροειδείς) είναι κωδικοποιημένες με χρώμα (λευκό, πορτοκαλί και κίτρινο, αντίστοιχα). (Β) Επίπεδα διαιτητικών φυτοχημικών που βρέθηκαν σε παιδιά με ΔΑΦ σε PRE (μπλε) και PEAK (ανοιχτό μπλε) και ομάδα TD (πράσινο) στις επικαλυπτόμενες κατηγορίες που περιγράφονται στο (Α). Κάθε περιοχή πλαισίου περικλείεται οριζόντια από το κάτω και το άνω τεταρτημόριο και υποδεικνύεται η διάμεσος (συμπαγή οριζόντια γραμμή εντός του πλαισίου). Οι επικαλυπτόμενες κατηγορίες υποδεικνύονται στην επάνω δεξιά γωνία. (Γ) Χρονικά εξαρτώμενα επίπεδα βιτεξίνης (απιγενίνη 8-γλυκοσίδη) που ανιχνεύθηκαν σε χρονικά σημεία PRE (10min πριν από τη θεραπεία με MC), PEAK, Post-1 και Post-2 (90, 180 και 270min μετά τη θεραπεία με MC, αντίστοιχα) ταυτότητα παιδιού A18. (Δ) Χρονικά εξαρτώμενα επίπεδα ρουτίνης (κερσετίνη 3-ρουτινοσίδη) που ανιχνεύθηκαν σε χρονικά σημεία που περιγράφονται στο (Γ) στο παιδί με ταυτότητα A16.
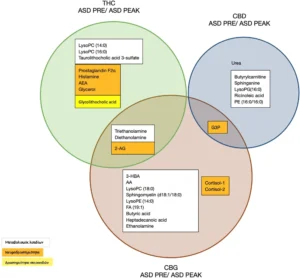
Εικόνα 3. Προσδιορισμός πιθανών βιοδεικτών που ανταποκρίνονται σε THC, CBD και CBG που διακρίνουν τους ασθενείς με ΔΑΦ σε PRE έναντι PEAK. Διάγραμμα Venn που απεικονίζει τους μοναδικούς και επικαλυπτόμενους βιοδείκτες που ανταποκρίνονται στην κάνναβη που ανταποκρίνονται (PRE/PEAK) στη θεραπεία THC, CBD και CBG. Οι λειτουργίες βιοδεικτών (μεταβολισμός λιπιδίων, νευροδραστηριότητα και δραστηριότητα στεροειδών) είναι κωδικοποιημένες με χρώμα (λευκό, πορτοκαλί και κίτρινο χαμηλά, αντίστοιχα).
Συζήτηση
Οι μεταβολικοί βιοδείκτες είναι δυναμικά συστατικά των κλάδων της ωμικής (γονιδιωματική, μεταγραφτομική, πρωτεομική και μεταβολομική) που είναι πιο κοντά στον φαινότυπο που μπορούν να ποσοτικοποιήσουν τις φυσιολογικές αλλαγές[10]. Αυτοί οι βιοδείκτες χρησιμοποιούνται με επιτυχία για τη διαστρωμάτωση ασθενών, τη διάγνωση, την παρακολούθηση, τη φαρμακοδυναμική / απόκριση και τα προγνωστικά εργαλεία[17]. Πρόσφατα αναφέραμε για βιοδείκτες στο σάλιο που ανταποκρίνονται στην κάνναβη, μεταβολίτες που μετρούν αντικειμενικά την ανταπόκριση στη θεραπεία MC σε παιδιά με ΔΑΦ και υποδεικνύουν τον αντίκτυπο σε σύγκριση με στοχευμένες τιμές που προσδιορίζονται σε πληθυσμό TD[14,15]. Οι βιοδείκτες που ανταποκρίνονται στην κάνναβη που παρέχουν ένα στιγμιότυπο υψηλής ανάλυσης των μεταβολικών αλλαγών που εξαρτώνται από τα κανναβινοειδή είναι το πλησιέστερο ποσοτικοποιήσιμο βήμα στη φαινοτυπική αξιολόγηση που χρησιμοποιείται επί του παρόντος σε παιδιά με ΔΑΦ. Χρησιμοποιώντας πληροφορίες από προγνωστικά ML που βασίζονται σε Gradient Boosting με τους περιορισμούς ενός μικρού συνόλου δεδομένων ασθενών, μπορέσαμε να χρησιμοποιήσουμε με επιτυχία τις σύνθετες διασταυρούμενες λειτουργίες (μεταβολίτες) και να προσδιορίσουμε την πιθανή επίδραση της θεραπείας με MC στον ρόλο των γνωστών και σχολιασμένων μεταβολικών οδών στο παιδιά με ΔΑΦ. Επιπλέον, μπορέσαμε να συσχετίσουμε νέους μη κανναβινοειδείς μεταβολίτες φυτικής προέλευσης με τη θεραπευτική επίδραση στην ομάδα θεραπείας με ΔΑΦ, η οποία δεν έχει αναφερθεί προηγουμένως.
Βιοδείκτες για τη διάκριση κατηγοριών παιδιών με ΔΑΦ με βάση την ανταπόκριση στη θεραπεία MC
Σε προηγούμενες μελέτες μας χρησιμοποιήσαμε διαφορετικούς αλγόριθμους στο ίδιο σύνολο δεδομένων για να εντοπίσουμε βιοδείκτες που ανταποκρίνονται στην κάνναβη χρησιμοποιώντας μια μεθοδολογία διαλογής και ταξινόμησης για ευεργετικά αποτελέσματα[14,15]. Οι προηγούμενοι αλγόριθμοι ελέγχθηκαν για μεταβολίτες που πληρούν τα ακόλουθα κριτήρια θεραπευτικής σημασίας, συγκεκριμένα: (1) αλλαγές ως προς την κάνναβη σε 60% ή περισσότερα παιδιά με ΔΑΦ. (2) επίπεδα μετά τη θεραπεία με MC (PEAK) σημαντικά διαφορετικά από το PRE και (3) ο υψηλότερος αριθμός παιδιών στα οποία τα επίπεδα μετατοπίστηκαν προς το φυσιολογικό εύρος που καθορίστηκε ως 2 τυπικές αποκλίσεις (SDEV) από τον μέσο όρο που βρέθηκε στην ομάδα TD. Σε αυτή τη μελέτη εφαρμόσαμε εργαλεία ML για τη διάκριση μεταξύ κατηγοριών παιδιών με ΔΑΦ στα PRE, PEAK και τον έλεγχο TD εστιάζοντας σε μοναδικούς μεταβολίτες που διαφοροποιούν τις κατηγορίες (πχ. PRE, PEAK, TD) ανεξάρτητα από το θετικό ή αρνητικό αποτέλεσμα.
Στην κατηγορία TD/ASD PRE/ASD PEAK, οι προγνωστικοί παράγοντες ML μπορούν να περιλαμβάνουν βιοδείκτες που εντοπίστηκαν στην προηγούμενη μελέτη που κινήθηκαν προς το εύρος TD (θεραπευτικά επωφελής) ή/και νέους βιοδείκτες που απομακρύνθηκαν από το εύρος TD (θεραπευτικά επιβλαβείς) μετά τη θεραπεία με MC. Εντοπίσαμε 7 μεταβολίτες στην κατηγορία TD /ASD PRE/ASD PEAK που είχαν προηγουμένως χαρακτηριστεί ως δυνητικοί βιοδείκτες που ανταποκρίνονται στην κάνναβη (Siani-Rose et al.[14] Suppl 1) με ρόλους στον μεταβολισμό των λιπιδίων[15] και συνδέονται με τη ΔΑΦ. Επιπλέον, δεν μπορέσαμε να βρούμε καμία ένδειξη αρνητικής επίδρασης του MC, δηλαδή ενός μεταβολίτη στον οποίο η κατανομή του δείγματος στην ομάδα PRE ήταν παρόμοια με την ομάδα TD και στη συνέχεια αυξήθηκε (μετατοπίστηκε από το εύρος TD) στο PEAK (Εικ. 1Β). Αυτό θα μπορούσε να εξηγηθεί από την επιλογή των παιδιών για την ομάδα ΔΑΦ που αντιμετωπίστηκαν επιτυχώς με MC υπό την επίβλεψη γιατρού.
Μεταξύ των τριών κατηγοριών που περιγράφονται στην Εικόνα 1, ο νευροδραστικός βιοδείκτης που ανταποκρίνεται στην κάνναβη με βάση τα λιπίδια LysoPE(18:1) ήταν ο μόνος διακριτικός παράγοντας και στις 3 κατηγορίες (ASD PRE/ASD PEAK, ASD PRE και ASD PEAK και TD/ASD PRE/ASD PEAK), το οποίο μπορεί να υποδεικνύει μερική επίδραση της θεραπείας με MC σε σημαντικές υποκείμενες παθήσεις της ΔΑΦ. Μη φυσιολογικά επίπεδα LysoPE(18:1) που ανιχνεύθηκαν στον ιππόκαμπο των αρουραίων είχαν προταθεί προηγουμένως ως δείκτης μεταισχαιμικής γνωστικής εξασθένησης[18]. Το ενδοκανναβινοειδές AEA ήταν ο μόνος παράγοντας διάκρισης μεταβολίτη στις κατηγορίες ASD PRE/ASD PEAK και ASD PRE και ASD PEAK αλλά όχι στην ομάδα TD. Το ΑΕΑ ανταποκρίνεται στο MC παρόμοια με όλους τους άλλους μεταβολίτες και επικαλύπτει τουλάχιστον 2 κατηγορίες που περιγράφονται στο Εικ. 1Β μειώνοντας το μεγάλο εύρος κατανομής δείγματος που ανιχνεύεται στο PRE στο μικρό εύρος κατανομής που λαμβάνεται στην ομάδα TD. Αυτή η αυστηρότερη κατανομή στο PEAK υποδηλώνει μείωση της ρύθμισης του ενδοκανναβινοειδούς AEA ως απόκριση στη θεραπεία με κανναβινοειδή, υποδηλώνοντας πιθανώς βελτιωμένο τόνο ΕΚΣ. Οι παρατηρήσεις μας υποστηρίζουν περαιτέρω τους Di Marzo et al.[19], όπου η επαναλαμβανόμενη θεραπεία με THC μείωσε την περιεκτικότητα και τη σηματοδότηση της βιοσυνθετικής πρόδρομης ουσίας Ν-αραχιδονοϋλφωσφατιδυλαιθανολαμίνης (NArPE) του ΑΕΑ στο ραβδωτό σώμα των αρουραίων.
Εντός των μοναδικών μεταβολιτών που λαμβάνονται ειδικά στην κατηγορία ASD PRE/ASD PEAK ή στην κατηγορία ASD PRE και ASD PEAK, μόνο η παλμιτοϋλοκαρνιτίνη, η HBA, η HVA και η κορτιζόλη πληρούσαν τα κριτήρια βιοδεικτών που ανταποκρίνονται στην κάνναβη που αναφέρθηκαν προηγουμένως (Siani-Rose et al.[14] Supp 1), ενώ όλα τα άλλα εντοπίστηκαν στην προηγούμενη μελέτη μας, αλλά δεν πληρούσαν τα πρώτα κριτήρια, συγκεκριμένα παρουσία σε 60% ή περισσότερα παιδιά[14]. Για παράδειγμα, η DHEA-S που σχετίζεται με την επιθετικότητα σε ψυχιατρικές διαταραχές[20] ανιχνεύθηκε σε υψηλά επίπεδα μόνο σε νεαρά άτομα εφήβους (αγόρια 11–12 ετών).
Μη κανναβινοειδή φυτοχημικά φυτά με πιθανές επιπτώσεις συνδυαστικής επίδρασης
Η ικανότητα αναγνώρισης μεταβολιτών που διακρίνουν το TD/ASD PRE/ASD PEAK μας επέτρεψε να συσχετίσουμε γνωστά φυτοχημικά φυτών με επιτυχή θεραπεία με MC που παρατηρήθηκε από γονική αξιολόγηση και είχε αναφερθεί προηγουμένως στο Siani-Rose et al.[14] Supp 3. Τα φυτοχημικά είναι δευτερογενείς μεταβολίτες φυτών, όπως οι πολυφαινόλες (πχ. φλαβονοειδή), τερπενοειδή (πχ. καροτενοειδή) και φυτοστερόλες (πχ. στερόλες) με φαρμακευτικές ιδιότητες όπως αντιφλεγμονώδεις, αντιοξειδωτικές και αντιβακτηριακές[21]. Τα μονοτερπένια κάνναβης, όπως το λιμονένιο, το μυρσένιο και η λιναλοόλη, που μοιράζονται τον κοινό πρόδρομο C-10 διφωσφορικό γερανυλεστέρα (GPP) με το CBGA, θεωρείται ότι παρέχουν μια συνεργατική δράση φυτοκανναβινοειδών-τερπενοειδών, γνωστή ως το συνδυαστική επίδραση[16]. Σε αυτή τη μελέτη, εντοπίσαμε 7 μόρια φυτικής προέλευσης, όλα τα διαιτητικά φυτοχημικά από 3 ομάδες που αναφέρθηκαν προηγουμένως ότι αναστέλλουν την ακετυλοχολινεστεράση: πολυφαινόλες (flavone[22], rutin[23], vitexin[24] και naringenin[25]), τερπενοειδή (ζεαξανθίνη[26] και κοροσολική στερόλη[27]) και φυτοστερόλες (σιτοστερόλη[27]) (Εικ. 2Α, Β). Δεδομένου ότι 6 φυτοχημικά (φλαβόνη, ρουτίνη, βιτεξίνη, ναριγγενίνη, ζεαξανθίνη και σιτοστερόλη) δεν ανιχνεύθηκαν στην ομάδα TD και εμφάνισαν αυξημένα επίπεδα στο PEAK, είναι δυνατόν να χαρακτηριστεί αυτή η ανασταλτική δράση της ακετυλοχολινεστεράσης (AchE) ως συνδυαστική επίδραση. Από αυτή την άποψη, η αναστολή της AChE από το φάρμακο γκαλανταμίνη αναφέρθηκε προηγουμένως ότι μειώνει αποτελεσματικά την ευερεθιστότητα και τον λήθαργο / κοινωνική απόσυρση σε παιδιά με ΔΑΦ[28].
Βιοδείκτες για τη διάκριση της συσχέτισης με κύρια κανναβινοειδή σε παιδιά με ΔΑΦ με βάση την ανταπόκριση στη θεραπεία με MC
Οι βιοδείκτες που ανταποκρίνονται στην κάνναβη που κατηγοριοποιούνται ειδικά κατά THC, CBD και CBG μπορούν να υποδεικνύουν τις μεταβολικές οδούς που επηρεάζονται από τα κανναβινοειδή σε παιδιά με ΔΑΦ (Εικ. 3). Αυτό είναι ένα προκαταρκτικό βήμα για την κατανόηση του MOA των κανναβινοειδών και μια πορεία προς την εξατομικευμένη θεραπεία με MC. Βρήκαμε ότι η THC αλληλεπιδρά με την οπισθοδρομική οδό σηματοδότησης κανναβινοειδών (KEGG map 04723, Kyoto Encyclopedia of Genes and Genomes, https://www.kegg.jp) αλλάζοντας τα επίπεδα των 2-AG και AEA. Η THC επομένως παίζει σημαντικό ρόλο στη σηματοδότηση κατά μήκος της συναπτικής σχισμής και στη σύνδεση και ενεργοποίηση του υποδοχέα CB1 που βρίσκεται τόσο στις νευρικές μεμβράνες στη σύναψη όσο και στη μιτοχονδριακή μεμβράνη στα διεγερτικά και ανασταλτικά άκρα[29]. Η CBG βρέθηκε να επηρεάζει μόνο τα επίπεδα της 2-AG, ενώ η CBD δεν επηρέασε κανένα από τα ενδοκανναβινοειδή, υποδηλώνοντας έναν διαφορετικό MOA. Επιπλέον, η THC, η CBD και η CBG προκαλούν αλλαγές στην οδό μεταβολισμού των γλυκεροφωσφολιπιδίων (KEGG map 00564) και η CBD και η CBG επηρεάζουν τον μεταβολισμό των σφιγγολιπιδίων (KEGG map 00600). Ενώ η THC αλλάζει τα επίπεδα των βιοδεικτών που βασίζονται σε λιπίδια, νευροδραστικά και στεροειδή, η CBD επηρέασε κυρίως τους βιοδείκτες που βασίζονται σε λιπίδια, όπως προτείνεται από τους Veilleux et al. μέσω του εκτεταμένου ΕΚΣ ή του endocannabinoidome (eCBome)[30]. Το CBGA, η όξινη μορφή της CBG, είναι επίσης ο πρόδρομος του THCA και του CBDA, που μετατρέπονται σε THC και CBD μέσω αποκαρβοξυλίωσης σε υψηλή θερμοκρασία. Η CBG ήταν λιγότερο συγκεκριμένη και μπορεί ενδεχομένως να λειτουργήσει ως “γέφυρα” μεταξύ THC και CBD με βάση τους επικαλυπτόμενους βιοδείκτες που ελήφθησαν σε αυτήν τη μελέτη. Αυτό προσθέτει υποστήριξη στα ευρήματα των Nachnani et al.[31], δηλαδή ότι “η CBG φαίνεται να βρίσκεται, φαρμακολογικά, μεταξύ THC και CBD”.
ML και διεύρυνση της γνώσης των μεταβολικών οδών
Λαμβάνοντας μαζί τα δεδομένα ML που ελήφθησαν σε αυτή τη μελέτη και τις γνωστές μεταβολικές οδούς των ενδοκανναβινοειδών[32], των λυσογλυκεροφωσφολιπιδίων[33], των σφιγγολιπιδίων[34] και της οξείδωσης των λιπαρών οξέων[35] στην ΔΑΦ[36], δείκτες κατάθλιψης[37] και μονοπάτια που περιέχουν ισταμίνη[38], καταφέραμε να συναρμολογήσουμε προκαταρκτικά την THC και την μεταβολική οδό που ανταποκρίνεται στην CBG σε παιδιά με ΔΑΦ (Εικ. 4). Εισαγάγαμε επίσης γενικούς βιοδείκτες που ανταποκρίνονται στην κάνναβη που περιγράφηκαν προηγουμένως στους Siani-Rose[14,15] σε αυτήν την απλοποιημένη μεταβολική οδό. Το ενδοκανναβινοειδές μεταβολικό μονοπάτι συνδέθηκε στενά με την THC, συμπεριλαμβανομένων και των δύο, του AEA και της 2-AG. Η CBG συσχετίστηκε με την 2-AG, το αραχιδονικό οξύ (AA) και την αιθανολαμίνη (ETA), ενώ το tETA και το diETA συσχετίστηκαν τόσο με THC όσο και με CBG.
Μελέτες υποδεικνύουν ότι η ΔΑΦ[36] και η Νόσος του Alzheimer[40] συνδέονται με αυξημένη δραστηριότητα της εγκεφαλικής φωσφολιπάσης Α2 (brain phospholipase A2, PLA2) που σχετίζεται με νευροφλεγμονή, η οποία μετατρέπει ειδικά τα φωσφολιπίδια της κυτταρικής μεμβράνης σε αραχιδονικό οξύ (arachidonic acid, ΑΑ). Ομοίως, οι Esvap & Ulgen[34] ανέφεραν αυξημένη δραστηριότητα υδρόλυσης PLA2 των φωσφολιπιδίων σε ΑΑ και πολυακόρεστα ελεύθερα λιπαρά οξέα (polyunsaturated fatty acids, PUFAs) σε παιδιά με ΔΑΦ. Από αυτή την άποψη, η συσχέτιση της CBG με το ΑΑ μπορεί να παρέχει μια εικόνα για τον αντιφλεγμονώδη ρόλο της μειώνοντας τα επίπεδα ΑΑ σε παιδιά με ΔΑΦ (PRE/PEAK) πιθανώς μέσω PLA2. Αυτό το συσχετιζόμενο με την CBG / AA συνδέθηκε επίσης με το μεταβολικό μονοπάτι που σχετίζεται με την THC που περιλαμβάνει 2-AG, προσταγλανδίνη F2α και γλυκερόλη, τα οποία εμπλέκονται στη ΔΑΦ[36] και στην κατάθλιψη[37].
Τα λυσογλυκεροφωσφολιπίδια υδρολύονται σε γλυκεροφωσφολιπιδικά λιπίδια που εμπλέκονται στη σηματοδότηση και στη βιοσύνθεση της μεμβράνης. Τα προκαταρκτικά μας δεδομένα έδειξαν ότι τα μέλη των οδών λυσογλυκεροφωσφολιπιδίου συνδέονται πιθανώς με THC (LysoPC), CBD (LysoPG) και CBG (LysoPE και LysoPC), τα οποία είναι όλα προϊόντα των ενζύμων φωσφολιπάσης Α (PLA) sPLA2, PLA2 και PLA2, αντίστοιχα[33]. Σημαντική αύξηση στη δραστηριότητα του PLA2 αναφέρθηκε προηγουμένως από τους Bell et al.[39] και από τους Qasem et al.[41], οι οποίοι εμφάνισαν μείωση στις μέσες συγκεντρώσεις PE και PC, των υποστρωμάτων LysoPE και LysoPC αντίστοιχα. Αυτό συμφωνεί με τις παρατηρήσεις μας που δείχνουν αυξημένα επίπεδα LysoPE και LysoPC στο PRE (Εικ. 1) που μειώθηκαν ως απόκριση στη θεραπεία με MC που περιέχει THC, CBD ή/και CBG. Οι Qasem et al.[41] πρότειναν ότι η φλεγμονή αυξάνει τα επίπεδα PLA2 μέσω μεσολαβητών σε απόκριση στο οξειδωτικό στρες σε παιδιά με ΔΑΦ. Είναι πιθανό ότι η THC, η CBD ή/και η CBG προλαμβάνουν τη φλεγμονή και επομένως μειώνουν τα επίπεδα του PLA2.
Η οδός βιοσύνθεσης των σφιγγολιπιδίων συσχετίστηκε με την CBD (σφιγγανίνη) και την CBG (σφιγγομυελίνη). Τρία λιπίδια στην οδό βιοσύνθεσης σφιγγολιπιδίων, συγκεκριμένα, σφιγγοσίνη, λακτοζυλοκεραμίδιο και ακετυλοσφιγγοσίνη, που ανιχνεύθηκαν σε υψηλά επίπεδα σε PRE σε παιδιά με ΔΑΦ, δεν συσχετίστηκαν με κανένα κανναβινοειδές (Εικ. 1). Ενώ στη μελέτη μας ελήφθησαν χαμηλά/μη ανιχνεύσιμα επίπεδα κεραμιδίου[14,15], τα υψηλά επίπεδα που ανιχνεύθηκαν στο άμεσο προϊόν της σφιγγοσίνης (Εικ. 1Β) και σφιγγομυελίνης (δεν φαίνεται) θα μπορούσαν να εξηγηθούν από την υψηλή παραγωγή κεραμιδίου που γρήγορα μετατράπηκε σε άλλα παράγωγα συμπεριλαμβανομένης της σφιγγοσίνης και της σφιγγομυελίνης. Οι Esvap & Ulgen[34], χρησιμοποιώντας δεδομένα μεταγραφικής για την ανάπτυξη ενός μεταβολικού μοντέλου σε κλίμακα γονιδιώματος ειδικής ΔΑΦ (GEM), πρότειναν ότι η βιοσύνθεση κεραμιδίου προκαλείται από το οξειδωτικό στρες σε παιδιά με ΔΑΦ και υδρολύεται γρήγορα. Τα δεδομένα μας υποστηρίζουν αυτήν την υπόθεση καθώς η θεραπεία με MC γενικά[14,15] και η CBD και η CBG σε αυτή τη μελέτη συνδέθηκαν με μειωμένο οξειδωτικό στρες.
Βάση δεδομένων ML βιοδεικτών και ανταπόκρισης στην κάνναβη
Η ανάπτυξη βιοδεικτών που ανταποκρίνονται στην κάνναβη είναι το πρώτο βήμα για να ποσοτικοποιηθεί αντικειμενικά ο αντίκτυπος της θεραπείας με MC. Παρουσιάζει επίσης μια ευκαιρία για την καλύτερη κατανόηση των σχέσεων μεταξύ αυτών των βιοδεικτών και των κανναβινοειδών χρησιμοποιώντας εφαρμογές ML και για την απόκτηση εικόνας για το MOA των ενεργών κανναβινοειδών σχετικά με τις υποκείμενες καταστάσεις της ΔΑΦ. Οι βιοδείκτες που ανταποκρίνονται στην κάνναβη παρέχουν ένα δυναμικό, υψηλής ανάλυσης και πλούσιο σύνολο δεδομένων σε διάφορες πτυχές, όπως φαίνεται σε αυτή τη μελέτη: (1) το ευρύ φάσμα επιπέδων ανίχνευσης, στο οποίο τα υψηλότερα ανιχνεύσιμα επίπεδα του μεταβολίτη γαλακτικού οξέος ήταν 19.000 φορές υψηλότερα από τα επίπεδα οξειδωμένου οξέος γλουταθειόνης σε μοριακή βάση, (2) ο μεγάλος αριθμός χαρακτηριστικών, δηλαδή οι μεταβολίτες και οι πιθανοί βιοδείκτες σε κάθε δείγμα, (3) κάθε παιδί είναι μια δυναμική (πριν και μετά τη θεραπεία) ανεξάρτητη μελέτη και (4) την ικανότητα ανάλυσης μεγάλου αριθμού συσχετίσεων, τόσο γραμμικών όσο και σύνθετων, μεταξύ ενός μεγάλου αριθμού χαρακτηριστικών και δειγμάτων. Αυτές οι τέσσερις πτυχές, που δημιουργούν ένα δυναμικό, υψηλής ανάλυσης και πλούσιο σύνολο δεδομένων για εφαρμογές ML, είναι το κλειδί για τον εντοπισμό νέων πιθανών βιοδεικτών, ακόμη και με χαμηλούς παράγοντες διάκρισης ή μόνο σε συνδυασμό με οποιονδήποτε αριθμό άλλων βιοδεικτών. Αυτό το σύνολο δεδομένων υποστηρίζει επίσης την εξατομικευμένη ιατρική προσέγγιση, ειδικά για τη θεραπεία με MC, καθώς οι μεταβολικές αλλαγές αντανακλούν τόσο γενετικούς όσο και περιβαλλοντικούς παράγοντες, με δείγματα πριν και μετά τη θεραπεία, που αποτελούν τη βάση ακριβών προβλέψεων ML για θεραπεία στο μέλλον.
Συμπεράσματα
Ενώ απαιτούνται περαιτέρω μελέτες μεγάλου μεγέθους δείγματος για την ανάπτυξη μιας μεγάλης στατιστικά ισχυρής βάσης δεδομένων, οι βιοδείκτες που ανταποκρίνονται στην κάνναβη σε συνδυασμό με τεχνικές ML που βασίζονται σε Gradient Boosting μπορούν να εξατομικεύσουν με επιτυχία τη θεραπεία MC που σχετίζεται με το ΕΚΣ. Μπορεί επίσης να παρέχει ένα μεταβολικό στιγμιότυπο στο οποίο η θεραπεία με MC μπορεί να χρησιμοποιηθεί ως ανιχνευτής για την ανάδειξη των μεταβολικών οδών που σχετίζονται με την ΔΑΦ μετατρέποντας προσωρινά την παθοφυσιολογία της ΔΑΦ στην ομοιόσταση. Επιπλέον, τα προκαταρκτικά μας αποτελέσματα υποδηλώνουν ότι οι εφαρμογές ML μπορούν να προσδιορίσουν το συγκεκριμένο MOA των κανναβινοειδών και την επίδραση των φυτοχημικών ουσιών στο περιβάλλον χωρίς να χρειάζεται να ελέγχεται το καθένα ξεχωριστά.
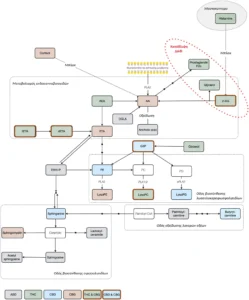
Εικόνα 4. Απλοποιημένες μεταβολικές οδοί που σχετίζονται με τη διαφορική έκφραση των πιθανών βιοδεικτών που ανταποκρίνονται στην κάνναβη στην ΔΑΦ μετά από θεραπεία με THC, CBD και CBG. Οι πιθανοί βιοδείκτες που ανταποκρίνονται στην κάνναβη στην ΔΑΦ ανταποκρίνονται άμεσα στην THC (πράσινο), CBD (μπλε) και CBG (καφέ) που βρίσκονται στις μεταβολικές οδούς των λυσογλυκεροφωσφολιπιδίων, των σφιγγολιπιδίων, της οξείδωσης λιπαρών οξέων, του ανανδαμιδίου και της αιθανολαμίνης-φωσφορικής (EthN-P) ενδείκνυται επίπτωση στη ΔΑΦ και την κατάθλιψη. Οι πιθανοί βιοδείκτες που ανταποκρίνονται στην κάνναβη της ΔΑΦ που είχαν προηγουμένως εντοπιστεί και περιγραφεί μόνο στο Siani-Rose (2021 και 2022) είναι γκρι, με τους μεταβολίτες σε λευκό.
Περιορισμοί
Αν και οι περιορισμοί στην πιλοτική μας μελέτη παρατήρησης συζητήθηκαν προηγουμένως στους Siani-Rose et al.[14] και Siani-Rose et al.[15], εξετάζουμε αρκετούς επιπλέον περιορισμούς σχετικά με αυτή τη μελέτη. Πρώτον, το μικρό μέγεθος δείγματος της ομάδας ΔΑΦ δεν αντιπροσωπεύει την πλήρη ετερογένεια του κλινικού φαινοτύπου που βρίσκεται σε ολόκληρο τον πληθυσμό της ΔΑΦ και επομένως δεν μπορούμε να προτείνουμε ότι η θεραπεία με MC είναι σχετική για όλα τα άτομα με ΔΑΦ. Δεύτερον, κάθε παιδί θεωρήθηκε ως μεμονωμένη περίπτωση που υποβλήθηκε σε θεραπεία με μοναδικό περιεχόμενο και θεραπευτική αγωγή κανναβινοειδών. Έτσι, η συσχέτιση των βιοδεικτών με την ισχύ των κανναβινοειδών περιορίζεται σε ένα εύρος συγκεντρώσεων που προσδιορίζονται αυθαίρετα και δεν αντιπροσωπεύει άμεση γραμμική συσχέτιση. Τρίτον, κάθε μελέτη παρατήρησης διεξήχθη σε μία ημέρα και αντιπροσωπεύει τη συμπεριφορά του παιδιού σε ένα μόνο χρονικό σημείο που μπορεί να μην αντικατοπτρίζει όλο το φάσμα των συμπεριφορών που επηρεάζονται από περιβαλλοντικούς παράγοντες και μπορεί να διαφέρουν από μέρα σε μέρα. Τέταρτον, ο πληθυσμός των βιοδεικτών είναι προκατειλημμένος προς τα παιδιά που αντιμετωπίζονται επιτυχώς με MC. Πέμπτον, οι γονείς χρησιμοποίησαν ένα σταγονόμετρο για να θεραπεύσουν τα παιδιά με μη-συνταγογραφημένο MC, το οποίο μπορεί να προκαλέσει ανακρίβεια στα επίπεδα της δόσης που αναφέρθηκαν. Έκτον, οι συγγραφείς δεν επαλήθευσαν την περιεκτικότητα σε κανναβινοειδή και την ισχύ της θεραπείας με MC που αναφέρθηκαν από τους γονείς. Έβδομο, δεδομένου ότι οι βιοδείκτες ανιχνεύθηκαν στο σάλιο, ορισμένοι μπορεί να μην αντιπροσωπεύουν τον σχετικό φυσιολογικό τους ρόλο. Όγδοο, το μικρό μέγεθος του συνόλου δεδομένων σε συνδυασμό με τον πολύ μεγαλύτερο αριθμό χαρακτηριστικών (μόρια) και την ετερογένεια του σχήματος δεν είναι βέλτιστο για την εκπαίδευση και, στη συνέχεια, την επικύρωση και τη δοκιμή των μοντέλων πρόβλεψης ML. Μια μελλοντική μελέτη για τη δημιουργία ενός συνόλου δεδομένων από μια μεγαλύτερη ομάδα ασθενών με περισσότερα δείγματα θα είναι απαραίτητη για την αντιμετώπιση αυτού του περιορισμού και την ανάπτυξη προγνωστικών μοντέλων που μπορούν να γενικευθούν, με σκοπό την ταξινόμηση δειγμάτων με ισχυρά επίπεδα ακρίβειας.
Λόγω της πολυπλοκότητας των μεταβολικών οδών και των σημερινών περιορισμών της συλλογικής μας γνώσης, όπως αναπαριστάται στη βάση δεδομένων KEGG, αναμένουμε τις προτεινόμενες απλουστευμένες διασταυρούμενες αλληλεπιδράσεις (Εικ. 4) να εξελιχθούν καθώς αποκαλύπτονται περισσότερες πληροφορίες μέσω παρόμοιων μελετών.
Μέθοδοι
Η μελέτη παρατήρησης για την αξιολόγηση της ανταπόκρισης των παιδιών με ΔΑΦ σε θεραπεία MC κατευθυνόμενη από τον γιατρό χρησιμοποιώντας κλίμακες μεταβολομικής σάλιου και αξιολόγησης συμπεριφοράς πραγματοποιήθηκε το 2020-2021. Τα πρωτόκολλα μελέτης εξετάστηκαν και εγκρίθηκαν από την Ethical and Independent Review Services, μια πιστοποιημένη θεσμική επιτροπή αναθεώρησης Association for the Accreditation of Human Research Protection Programs, Inc. (AAHRPP) (αναφ. 20114-01X). Επιβεβαιώνουμε ότι όλες οι μέθοδοι πραγματοποιήθηκαν σύμφωνα με τις σχετικές οδηγίες και κανονισμούς. Οι γονείς/κηδεμόνες των συμμετεχόντων παιδιών υπέγραψαν ένα έντυπο συγκατάθεσης κατόπιν ενημέρωσης και τα παιδιά TD από την ομάδα ελέγχου υπέγραψαν ένα έντυπο συγκατάθεσης. Οι συμμετέχοντες, ο σχεδιασμός της μελέτης, η απόκτηση δεδομένων και η αξιολόγηση της γονικής συμπεριφοράς, περιγράφηκαν λεπτομερώς στους Siani-Rose et al.[14] και Siani-Rose et al.[15], και εν συντομία παρακάτω.
Συμμετέχοντες
Οι συμμετέχοντες της ομάδας ΔΑΦ (n = 15), μέση ηλικία 9,4 έτη, αναλογία αρσενικών:θηλυκών 8:1, στρατολογήθηκαν μέσω των CannaCenters Wellness and Education (Lawndale, CA) και Whole Plant Access for Autism (WPA4A, μια μη κερδοσκοπική εταιρεία 501c3, Canyon Lake, CA). Τα κριτήρια συμπερίληψης ήταν: (1) ΔΑΦ που διαγνώστηκε από εξειδικευμένο επαγγελματία υγείας, (2) Θεραπεία MC υπό την επίβλεψη ιατρού για τουλάχιστον ένα χρόνο, (3) ηλικία μεταξύ 6 και 12 ετών και (4) δυνατότητα παροχής έως και τεσσάρων δειγμάτων σάλιου (0,5ml το καθένα) χρησιμοποιώντας τη μέθοδο παθητικού σάλιου χωρίς ενόχληση. Τα κριτήρια αποκλεισμού ήταν: (1) παιδιά που χρειάζονται κάνναβη συχνότερα από κάθε 8 ώρες. (2) τραυματική εγκεφαλική βλάβη με οποιαδήποτε γνωστή γνωστική συνέπεια ή απώλεια συνείδησης για περισσότερο από 5 λεπτά και (3) διάγνωση επιληψίας.
Οι συμμετέχοντες στην ομάδα TD (n = 10), μέση ηλικία 9,3 έτη, αναλογία αρσενικών:θηλυκών 9:1, στρατολογήθηκαν μέσω μιας διαδικτυακής ομάδας γονέων στο Σαν Φρανσίσκο και τα κριτήρια ένταξης ήταν τα εξής: (1) χωρίς ειδικές εκπαιδευτικές ανάγκες και (2 ) κανένα άτομο ή μέλος της άμεσης οικογένειας δεν έχει διαγνωστεί με αναπτυξιακές διαταραχές.
Σχεδιασμός μελέτης
Όλοι οι συμμετέχοντες στην ομάδα TD παρείχαν δείγματα στα χρονικά σημεία: PRE – πρωί, πριν από τη θεραπεία με MC. και PEAK – όταν η θεραπεία θεωρήθηκε από τους γονείς ότι έφθασε στο μέγιστο αποτέλεσμα με βάση τις παρατηρήσεις τους πριν από τη μελέτη, περίπου 90 λεπτά μετά τη θεραπεία με MC. Ορισμένοι από τους συμμετέχοντες της ομάδας ΔΑΦ έδωσαν επίσης δείγματα σε χρονικά σημεία Μετά-1 και Μετά-2, περίπου 180 και 270 λεπτά μετά τη θεραπεία με MC, αντίστοιχα. Η ομάδα ελέγχου TD έδωσε ένα δείγμα σάλιου το πρωί.
Για να διασφαλιστεί η υψηλή αναπαραγωγιμότητα των αποτελεσμάτων, η μελέτη διεξήχθη ως εξής: (1) Οι συμμετέχοντες της ομάδας ΔΑΦ δεν υποβλήθηκαν σε θεραπεία με MC για τουλάχιστον 8 ώρες πριν από την PRE (περίοδος έκπλυσης), (2) όλοι οι συμμετέχοντες δεν κατανάλωναν υψηλή περιεκτικότητα σε ζάχαρη, οξύ και καφεΐνη 1 ώρα πριν από οποιαδήποτε συλλογή δείγματος σάλιου, (3) όλοι οι συμμετέχοντες ξέπλυναν το στόμα τους 20 λεπτά πριν από τη συλλογή σάλιου, (4) οι γονείς όλων των συμμετεχόντων συμπλήρωσαν σύντομη κλίμακα συμπεριφοράς Likert 10 λεπτά πριν από κάθε συλλογή δείγματος σάλιου και (5) όλα τα δείγματα σάλιου συλλέχθηκαν χρησιμοποιώντας το κιτ συλλογής παθητικής στρίμωξης (Salimetrics, Carlsbad, CA), όπως περιγράφηκε προηγουμένως λεπτομερώς στο Siani-Rose et al.[14].
Μη στοχευμένη μεταβολομική ανάλυση
Αμέσως μετά τη συλλογή όλα τα δείγματα σάλιου αποθηκεύτηκαν προσωρινά (έως 24 ώρες) στους –20°C και στη συνέχεια μεταφέρθηκαν στους –80°C μέχρι την capillary electrophoresistime-of-flightmass spectrometry (CE-TOF-MS) και rapid resolution liquid chromatography-time-of-flightmass spectrometry (RRLC-TOF-MS) που πραγματοποιήθηκε από την Human Metabolome Technologies, Inc. (HMT, Tsuruoka, Ιαπωνία) και υποβλήθηκε σε επεξεργασία όπως περιγράφηκε προηγουμένως λεπτομερώς στο Siani-Rose et al.[14].
Πηγή δεδομένων
Η προετοιμασία δειγμάτων, η ανίχνευση και η ταυτοποίηση μεταβολιτών και η ανάλυση ποιοτικού ελέγχου δημοσιεύθηκαν προηγουμένως στο Siani-Rose et al.[14]. Τα δεδομένα μεταβολομικής αποτελούνται από ενώσεις που ανιχνεύθηκαν σε 40 δείγματα σάλιου που συλλέχθηκαν από: 15 παιδιά με ΔΑΦ (15 δείγματα στο PRE, 15 αντίστοιχα δείγματα στο PEAK) και 10 δείγματα από την ομάδα ελέγχου TD.
Προεπεξεργασία δεδομένων
Προκειμένου να προσαρμοστούν τα δεδομένα σε μεταγενέστερη ανάλυση ML, εφαρμόστηκε η ακόλουθη προεπεξεργασία: (1) Κάθε καταχώρηση ένωσης που δεν ανιχνεύτηκε σε ένα δείγμα αντικαταστάθηκε από 0. Αυτό επέτρεψε τη χρήση αλγορίθμων που δεν μπορούν να επεξεργαστούν τις τιμές που λείπουν, ενώ εξακολουθούν να χρησιμοποιούν όλο το σύνολο δεδομένων. Ένα σημαντικό μέρος του συνόλου δεδομένων παρουσιάζει τέτοιες μη ανιχνευμένες εγγραφές σύνθετων για ένα ή περισσότερα παιδιά. Μια μη ανιχνευμένη ένωση υποδεικνύει παρουσία σε ένα δείγμα κάτω από το επίπεδο ανίχνευσης, και επομένως η αντικατάσταση της με 0 δεν αλλάζει θεμελιωδώς τα αποτελέσματα που αναμένουμε να λάβουμε από την ανάλυση μας. (2) Οι τιμές κανονικοποιήθηκαν για κάθε μεμονωμένη ένωση σε όλο το σύνολο δεδομένων σε ένα εύρος (0, 1).
Προετοιμασία συνόλου δεδομένων
Τέσσερα διαφορετικά σύνολα δεδομένων συντάχθηκαν για τις διάφορες αναλύσεις ML: (1) Πλήρες – ένα σύνολο δεδομένων που αποτελείται και από τα 40 δείγματα. (2) ASD – ένα σύνολο δεδομένων που αποτελείται μόνο από τα 30 δείγματα που συλλέχθηκαν από παιδιά με ΔΑΦ. (3) ASD PRE και ASD PEAK – ένα σύνολο δεδομένων 15 καταχωρήσεων που αποτελείται από τη συνένωση των δεδομένων PRE και μια διαφορά ανά ένωση μεταξύ δεδομένων PRE και PEAK, που αναφέρονται ως συγχωνευμένα δεδομένα PRE + PEAK. Αυτό το σύνολο δεδομένων περιέχει 2 x 645 = 1290 χαρακτηριστικά (ή μόρια) ανά δείγμα και (4) ASD PRE/ASD PEAK – ένα σύνολο δεδομένων 15 καταχωρήσεων που αποτελείται από μια διαφορά ανά ένωση μεταξύ δεδομένων PRE και δεδομένων PEAK για κάθε παιδί στην ομάδα ΔΑΦ.
Τα αριθμητικά σύνολα δεδομένων συμπληρώθηκαν με την προσθήκη συμπληρωματικών δεδομένων συμπεριφοράς έρευνας. Αυτά τα δεδομένα της έρευνας μετά τη θεραπεία μετατράπηκαν σε τρεις κατηγορίες αποτελεσμάτων: (1) βελτιωμένη συμπεριφορά, (2) μερικώς βελτιωμένη συμπεριφορά και (3) επιδείνωση της συμπεριφοράς. Αυτά τα δεδομένα της έρευνας χρησιμοποιούνται μαζί με προηγούμενη γνώση σχετικά με το ποια δείγματα ανήκουν σε παιδιά στην ομάδα TD ή ASD PRE για τη δημιουργία των στόχων πρόβλεψης για την εκπαίδευση των μοντέλων ML (Πίνακας 1). Τα δεδομένα περιελάμβαναν επίσης τις συγκεντρώσεις ενεργών κανναβινοειδών στη θεραπεία κάθε παιδιού στην ομάδα ΔΑΦ με τη μορφή αριθμητικών κλιμάκων (Πίνακας 1) για κάθε δείγμα PEAK.
Εργασίες πρόβλεψης ML
Οι εργασίες πρόβλεψης που περιγράφονται παρακάτω σχεδιάστηκαν για την αξιολόγηση της προβλεψιμότητας της κατηγορίας ενός δείγματος από το σύνολο δεδομένων, καθώς και για τον εντοπισμό πιθανών υποψήφιων ενώσεων ενδιαφέροντος που επιτρέπουν αυτές τις προβλέψεις.
Το πλήρες σύνολο δεδομένων εφαρμόστηκε για μοντέλα εκπαίδευσης για τις εργασίες ML της ταξινόμησης δειγμάτων ως TD, ASD PRE ή μία από τις τρεις κατηγορίες αποτελεσμάτων ASD PEAK (δηλαδή, βελτιωμένη συμπεριφορά, μερικώς βελτιωμένη συμπεριφορά ή επιδείνωση της συμπεριφοράς). Το σύνολο δεδομένων ΔΑΦ εφαρμόστηκε για μοντέλα εκπαίδευσης για τις εργασίες ML της ταξινόμησης δειγμάτων ως ASD PRE ή ως μία από τις τρεις κατηγορίες αποτελεσμάτων ASD PEAK. Το συγχωνευμένο σύνολο δεδομένων ASD PRE και ASD PEAK εφαρμόστηκε για μοντέλα εκπαίδευσης για τις εργασίες ML της ταξινόμησης άτυπων δειγμάτων σε μία από τις τρεις κατηγορίες αποτελεσμάτων ASD PEAK. Το σύνολο δεδομένων ASD PRE/ASD PEAK εφαρμόστηκε για μοντέλα εκπαίδευσης για τις εργασίες ML της ταξινόμησης δειγμάτων ΔΑΦ σύμφωνα με τα ενεργά κανναβινοειδή που υπάρχουν στη θεραπεία και τη δοσολογία τους, με βάση τις πληροφορίες σύνθεσης θεραπείας. Τα προβλεπόμενα ενεργά κανναβινοειδή περιελάμβαναν THC που κυμαίνεται από 0 έως 50mg ανά θεραπεία, CBD που κυμαίνεται από 0 έως 200mg ανά θεραπεία και CBG που κυμαίνεται από 0 έως 50mg ανά θεραπεία. Το σύνολο δεδομένων ASD PRE και ASD PEAK εφαρμόστηκε επίσης για μοντέλα εκπαίδευσης για την ίδια εργασία ML.
Ανάλυση εξόδου ML
Ο βασικός αλγόριθμος που χρησιμοποιήθηκε για τις διάφορες εργασίες πρόβλεψης που περιγράφονται παραπάνω ήταν η υλοποίηση Gradient Boosting[42] από το πακέτο Scikit-learn. Αυτός ο αλγόριθμος παρέχει, μετά την εκπαίδευση ενός μοντέλου για μια εργασία πρόβλεψης, μια βαθμολογία για τη χρησιμότητα κάθε χαρακτηριστικού του συνόλου δεδομένων εκπαίδευσης για τις εργασίες πρόβλεψης.
Ο περιορισμένος αριθμός δειγμάτων (έλεγχος ΔΑΦ ή TD) στα σύνολα δεδομένων σε συνδυασμό με τον πολύ μεγαλύτερο αριθμό χαρακτηριστικών (μόρια) δεν ήταν ο βέλτιστος για εκπαίδευση και στη συνέχεια εκτελέστηκε επικύρωση και δοκιμή των μοντέλων πρόβλεψης. Ως εκ τούτου, η συνάφεια των μοντέλων που εκπαιδεύονται σε κάθε εργασία για μελλοντική πρόβλεψη είναι περιορισμένη, καθώς τα μοντέλα που εκπαιδεύονται πιθανότατα υπερκαλύπτουν το σύνολο δεδομένων (βαθμολογία F1 ίση με 1 για όλα τα εκπαιδευμένα μοντέλα). Μια μελλοντική μελέτη για τη δημιουργία ενός μεγαλύτερου συνόλου δεδομένων με πολλά περισσότερα Θα είναι απαραίτητα δείγματα για την αντιμετώπιση αυτού του περιορισμού και την ανάπτυξη μοντέλων με σκοπό την ταξινόμηση δειγμάτων με ισχυρά επίπεδα ακρίβειας. Ωστόσο, τα μοντέλα που εκπαιδεύονται στο παρόν σύνολο δεδομένων μπορούν να παρέχουν πληροφορίες για τα δεδομένα υψηλών διαστάσεων και να προσδιορίζουν συγκεκριμένους μεταβολίτες (από τους 645) σημαντικούς για πρόβλεψη και πληροφορίες σχετικά με τις εμπλεκόμενες οδούς. Ως εκ τούτου, εστιάσαμε στους πιο σημαντικούς μεταβολίτες που προσδιορίστηκαν για καθένα από τα σενάρια πρόβλεψης που περιγράφονται παραπάνω.
Η κατάταξη σημαντικότητας (σημασία Gini) υπολογίζεται ως η κανονικοποιημένη συνολική μείωση του κριτηρίου που προκύπτει από αυτό το χαρακτηριστικό. Αυτή η κατάταξη σημασίας χαρακτηριστικών αντιπροσωπεύει τη συμβολή κάθε χαρακτηριστικού στη βελτίωση της προγνωστικής ικανότητας του μοντέλου μέσω της δημιουργίας του ενισχυμένου δέντρου αποφάσεων του μοντέλου. Αν και αντανακλά τη σημασία των χαρακτηριστικών στο τελικό μοντέλο, είναι αδύνατο να αξιολογηθεί η σχέση μεταξύ του χαρακτηριστικού και των προβλέψεων του μοντέλου. Η σημασία των χαρακτηριστικών έχει χρησιμοποιηθεί στο παρελθόν με επιτυχία στο πλαίσιο της ιατρικής έρευνας κατά τη χρήση προγνωστικών μηχανικής μάθησης που βασίζονται σε Gradient Boosting. Οι εφαρμογές που αναφέρθηκαν προηγουμένως περιλαμβάνουν πρόβλεψη έκβασης ασθενών στη μονάδα εντατικής θεραπείας, όπου η σημασία των χαρακτηριστικών επέτρεψε την παρουσίαση των κορυφαίων χαρακτηριστικών στους κλινικούς ιατρούς για να συγκρίνουν τη συνάφεια διαφορετικών μοντέλων στα μοντέλα πρόβλεψης και να χαρακτηρίσουν περαιτέρω την απόδοση των μοντέλων πρόβλεψης[43], καθώς και την πρόβλεψη κινδύνου για το οξύ στεφανιαίο σύνδρομο, για την εκτέλεση επιλογής χαρακτηριστικών για εκπαίδευση μοντέλων μηχανικής μάθησης μέσω μιας επαναληπτικής διαδικασίας για την επιλογή του βέλτιστου συνόλου χαρακτηριστικών[44].
Σε αυτή τη μελέτη, τα χαρακτηριστικά που αντιστοιχούν στους 645 διακριτούς μεταβολίτες (που ταυτοποιήθηκαν με CE-TOF-MS και RRLC-TOF-MS στο σάλιο) αξιολογήθηκαν για όλα τα δείγματα. Από αυτά τα χαρακτηριστικά, τα κορυφαία 50 χαρακτηριστικά κατάταξης σε σημασία για κάθε εργασία πρόβλεψης (το κορυφαίο 7,7% όλων των διαθέσιμων χαρακτηριστικών) λήφθηκαν υπόψη για τον προσδιορισμό των ενώσεων ενδιαφέροντος.
Δηλώσεις δεοντολογίας
Αυτή η μελέτη εγκρίθηκε από τις υπηρεσίες Ethical and Independent Review Services (E&I, Lees Summit, MO), οι μέθοδοι διεξήχθησαν σύμφωνα με τις σχετικές οδηγίες και κανονισμούς της έρευνας σε ανθρώπινα υποκείμενα. Λήφθηκε ενημερωμένη συγκατάθεση από τους γονείς/κηδεμόνες όλων των συμμετεχόντων παιδιών και η συγκατάθεση ελήφθη από τυπικά αναπτυσσόμενα παιδιά.
Διαθεσιμότητα δεδομένων
Τα σύνολα δεδομένων που χρησιμοποιούνται ή/και αναλύονται σε αυτήν τη μελέτη είναι διαθέσιμα από τον αντίστοιχο συγγραφέα κατόπιν εύλογου αιτήματος.
Βιβλιογραφικές αναφορές
[1]. American Psychiatric Association. Diagnostic and statistical manual of mental disorders: DSM-5. Arlington, VA The American Psychiatric Association APA (2013).
[2]. Parker, W. et al. The role of oxidative stress, inflammation and acetaminophen exposure from birth to early childhood in the induction of autism. J. Int. Med. Res. 45, 407–438 (2017).
[3]. DeFilippis, M. Depression in children and adolescents with autism spectrum disorder. Children 5, 112. https://doi.org/10.3390/children5090112 (2018).
[4]. Siniscalco, D., Schultz, S., Brigida, A. L. & Antonucci, N. Inflammation and neuro-immune dysregulations in autism spectrum disorders. Pharmaceuticals 11, 56. https://doi.org/10.3390/ph11020056 (2018).
[5]. Regev, O. et al. Association between ultrasonography foetal anomalies and autism spectrum disorder. Brain 145, 4519–4530 (2022).
[6]. Courchesne, E. et al. The ASD living biology: From cell proliferation to clinical phenotype. Mol. Psychiatry 24, 88–107 (2019).
[7]. Frye, R. E. et al. Emerging biomarkers in autism spectrum disorder: A systematic review. Ann. Transl. Med. 7, 792. https://doi.org/10.21037/atm.2019.11.53 (2019).
[8]. Ristori, M. V. et al. Proteomics and metabolomics approaches towards a functional insight onto autism spectrum disorders: phenotype stratification and biomarker discovery. Int. J. Mol. Sci. 21, 6274. https://doi.org/10.3390/ijms21176274 (2020).
[9]. Greener, J. G., Kandathil, S. M., Moffat, L. & Jones, D. T. A guide to machine learning for biologists. Nat. Rev. Mol. Cell. Biol. 23, 40–55 (2022).
[10]. Galal, A., Marwa, T. & Ahmed, M. Applications of machine learning in metabolomics: Disease modeling and classification. Front. Genet. 13, 3340. https://doi.org/10.3389/fgene.2022.1017340 (2022).
[11]. Chen, Q., Qiao, Y., Xu, X. J., You, X. & Tao, Y. Urine organic acids as potential biomarkers for autism-spectrum disorder in Chinese children. Front. Cell. Neurosci. 13, 150. https://doi.org/10.3389/fncel.2019.00150 (2019).
[12]. Hacohen, M. et al. Children and adolescents with ASD treated with CBD-rich cannabis exhibit significant improvements particularly in social symptoms: An open label study. Transl. Psychiatry 12, 375. https://doi.org/10.1038/s41398-022-02104-8 (2022).
[13]. Aran, A., Cassuto, H., Lubotzky, A., Wattad, N. & Hazan, E. Brief report: cannabidiol-rich cannabis in children with autism spectrum disorder and severe behavioral problems-a retrospective feasibility study. J. Autism Dev. Disord. 49, 1284–1288 (2019).
[14]. Siani-Rose, M. et al. Cannabis-responsive biomarkers: A pharmacometabolomics-based application to evaluate the impact of medical cannabis treatment on children with autism spectrum disorder. Cannabis Cannabinoid Res. 8, 126–137 (2023).
[15]. Siani-Rose, M. et al. The potential of salivary lipid-based Cannabis-responsive biomarkers to evaluate medical cannabis treatment in children with autism spectrum disorder. Cannabis Cannabinoid Res. https://doi.org/10.1089/can.2021.0224 (2022).
[16]. Russo, E. B. Taming THC: potential cannabis synergy and phytocannabinoid-terpenoid entourage effecs. Br. J. Pharmacol. 163, 1344–1364 (2011).
[17]. Califf, R. M. Biomarker definitions and their applications. Exp. Biol. Med. 243, 213–221 (2018).
[18]. Sabogal-Guaqueta, A. M., Villamil-Ortiz, J. G., Arias-Londono, J. D. & Cardona-Gomez, G. P. Inverse phosphatidylcholine / phosphatidylinositol levels as peripheral biomarkers and phosphatidylcholine / lysophosphatidylethanolamine-phosphatidylserine as hippocampal indicator of postischemic cognitive impairment in rats. Front. Neurosci. 12, 989. https://doi.org/10.3389/fnins.2018.00989 (2018).
[19]. Di Marzo, V. et al. Enhancement of anandamide formation in the limbic forebrain and reduction of endocannabinoid contents in the striatum of Δ9-tetrahydrocannabinol-tolerant rats. J. Neurochem. 74, 1627–1635 (2000).
[20]. Barzman, D. H., Patel, A., Sonnier, L. & Strawn, J. R. Neuroendocrine aspects of pediatric aggression: Can hormone measures be clinically useful?. Neuropsychiatr. Dis. Treat. 6, 691–697 (2010).
[21]. Upadhyay, S. & Madhulika, D. Role of polyphenols and other phytochemicals on molecular signaling. Oxid. Med. Cell Longev. 504253. https://doi.org/10.1155/2015/504253 (2015).
[22]. Uriarte-Pueyo, I. & Calvo, M. I. Flavonoids as acetylcholinesterase inhibitors. Curr. Med. Chem. 18, 5289–5302 (2011).
[23]. Amat-ur-Rasool, H. et al. Potential nutraceutical properties of leaves from several commonly cultivated plants. Biomolecules 10, 1556. https://doi.org/10.3390/biom10111556 (2020).
[24]. Sheeja Malar, D., Beema Shafreen, R., Karutha Pandian, S. & Pandima Devi, K. Cholinesterase inhibitory, anti-amyloidogenic and neuroprotective effect of the medicinal plant Grewia tiliaefolia-an in vitro and in silico study. Pharm. Biol. 55, 381–393 (2017).
[25]. Ali, M. Y. et al. Flavanone glycosides inhibit β-site amyloid precursor protein cleaving enzyme 1 and cholinesterase and reduce Aβ aggregation in the amyloidogenic pathway. Chem. Biol. Interact. 309, 108707. https://doi.org/10.1016/j.cbi.2019.06.020 (2019).
[26]. El-Baz, F. K., Abdel Jaleel, G. A., Hussein, R. A. & Saleh, D. O. Dunalialla salina microalgae and its isolated zeaxanthin mitigate age-related dementia in rats: Modulation of neurotransmission and amyloid-β protein. Toxicol. Rep. 8, 1899–1908 (2021).
[27]. Bahadori, M. B., Dinparast, L., Valizadeh, H., Farimani, M. M. & Ebrahimi, S. N. Bioactive constituents from roots of Salvia syriaca L.: Acetylcholinesterase inhibitory activity and molecular docking studies. S. Afr. J. Bot. 106, 1–4 (2016).
[28]. Ghaleiha, A. et al. Galantamine efficacy and tolerability as an augmentative therapy in autistic children: A randomized, double-blind, placebo-controlled trial. J. Psychopharmacol. 28, 677–685 (2014).
[29]. Zou, S. & Ujendra, K. Cannabinoid receptors and the endocannabinoid system: signaling and function in the central nervous system. Int. J. Mol. Sci. 19, 833 (2018).
[30]. Veilleux, A. D., Marzo, V. & Silvestri, C. The expanded endocannabinoid system/endocannabinoidome as a potential target for treating diabetes mellitus. Curr. Diabetes Rep. 19, 1–12 (2019).
[31]. Nachnani, R., Raup-Konsavage, W. M. & Vrana, K. E. The pharmacological case for cannabigerol. J. Pharmacol. Exp. Ther. 376, 204–212 (2021).
[32]. Maccarrone, M. Phytocannabinoids and endocannabinoids: Different in nature. Rend. Lincei Sci. Fis. Nat. 31, 931–938 (2020).
[33]. Tan, S. T., Ramesh, T., Toh, X. R. & Nguyen, L. N. Emerging roles of lysophospholipids in health and disease. Prog. Lipid Res. 80, 101068. https://doi.org/10.1016/j.plipres.2020.101068 (2020).
[34]. Esvap, E. & Ulgen, K. O. Neuroinflammation, energy and sphingolipid metabolism biomarkers are revealed by metabolic modeling of autistic brains. Biomedicines 11, 583. https://doi.org/10.3390/biomedicines11020583 (2023).
[35]. Tracey, T. J., Steyn, F. J., Wolvetang, E. J. & Ngo, S. T. Neuronal lipid metabolism: Multiple pathways driving functional outcomes in health and disease. Front. Mol. Neurosci. 11, 10. https://doi.org/10.3389/fnmol.2018.00010 (2018).
[36]. Yui, K., Imataka, G. & Yoshihara, S. Lipid-based molecules on signaling pathways in autism spectrum disorder. Int. J. Mol. Sci. 23, 9803 (2022).
[37]. Yui, K., Imataka, G., Nakamura, H., Ohara, N. & Naito, Y. Eicosanoids derived from arachidonic acid and their family prostaglandins and cyclooxygenase in psychiatric disorders. Curr. Neuropharmacol. 13, 776–785 (2015).
[38]. Pini, A. et al. The role of cannabinoids in inflammatory modulation of allergic respiratory disorders, inflammatory pain and ischemic stroke. Curr. Drug Targets 13, 984–993 (2012).
[39]. Bell, J. G. et al. Essential fatty acids and phospholipase A2 in autistic spectrum disorders. Prostaglandins Leukot. Essent. Fatty Acids. 71, 201–204 (2004).
[40]. Sanchez-Mejia, R. O. & Lennart, M. Phospholipase A2 and arachidonic acid in Alzheimer’s disease. BBA Mol. Cell Biol. Lipids 1801, 784–790 (2010).
[41]. Qasem, H. et al. Increase of cytosolic phospholipase A2 as hydrolytic enzyme of phospholipids and autism cognitive, social and sensory dysfunction severity. Lipids Health Dis. 16, 1. https://doi.org/10.1186/s12944-016-0391-4 (2017).
[42]. Friedman, J. H. Greedy function approximation: A gradient boosting machine. Ann. Stat. 1, 1189–1232 (2001).
[43]. Chen, T. et al. Prediction of extubation failure for intensive care unit patients using light gradient boosting machine. IEEE. Access 7, 150960–150968 (2019).
[44]. Lin, H., Xue, Y., Chen, K., Zhong, S. & Chen, L. Acute coronary syndrome risk prediction based on gradient boosted tree feature selection and recursive feature elimination: A dataset-specific modeling study. PLoS ONE 17, 11. https://doi.org/10.1371/journal.Pone.0278217 (2022).
Ευχαριστίες
Οι συγγραφείς της μελέτης επιθυμούν να αναγνωρίσουν τη συμβολή του συνιδρυτή της Cannformatics κ. Keneth Epstein για την επικοινωνία των συμμετεχόντων και τη συλλογή δειγμάτων. Ευχαριστούμε θερμά τα παιδιά και τις οικογένειες τους που συμμετείχαν σε αυτή τη μελέτη. Ευχαριστούμε επίσης τον κ. Ray Mirzabegian από την Canniatric, και την κυρία Rhonda Moeller και την κυρία Jenni Mai από το Whole Plant Access for Autism (WPA4A), για την οικονομική υποστήριξη και βοήθειά τους.
Συνεισφορές συγγραφέων
J.C.Q., M.S.R. και I.K: ανέπτυξαν την έννοια της έρευνας, σχεδίασαν τη μελέτη και συνέλεξαν τα δεδομένα. J.C.Q., M.S.R., R.M. και I.K: επεξεργάστηκαν και επικύρωσαν τα δεδομένα. J.C.Q., M.S.R., R.M., B.G. και Ι.Κ: ανέλυσαν τα δεδομένα. J.C.Q., M.S.R., R.M., B.G., M.T. και Ι.Κ.: συνέταξαν και εξέτασαν το χειρόγραφο.
Ανταγωνιστικά συμφέροντα
Ο κ. McKee και ο Dr. Kurek είναι συνιδρυτές και υπάλληλοι της Cannformatics. Ο κ. Siani-Rose είναι υπάλληλος της Cannformatics. Ο κ. Quillet είναι σύμβουλος στην Cannformatics. Ο Dr. Goldstein και ο Dr. Taylor είναι επιστημονικοί σύμβουλοι της Cannformatics. Οι συγγραφείς δηλώνουν ότι δεσμεύονται από συμφωνίες εμπιστευτικότητας που τους εμποδίζουν να αποκαλύψουν τα οικονομικά τους συμφέροντα σε αυτό το έργο.
Επιπλέον πληροφορίες
Η αλληλογραφία και τα αιτήματα για υλικά θα πρέπει να απευθύνονται στον Ι.Κ.
Πληροφορίες για τις ανατυπώσεις και τις άδειες είναι διαθέσιμες στη διεύθυνση www.nature.com/reprints
Σημείωση του εκδότη του Springer Nature ότι παραμένει ουδέτερο όσον αφορά τις διεκδικήσεις δικαιοδοσίας σε δημοσιευμένους χάρτες και θεσμικές σχέσεις.
Ανοιχτή πρόσβαση
Αυτό το άρθρο χορηγείται με άδεια Creative Commons Attribution 4.0 International, http://creativecommons.org/licenses/by/4.0/

 (η μελέτη σε μορφή αρχείου PDF)
(η μελέτη σε μορφή αρχείου PDF)